Aturan Oktet
Atom-atom unsur gas mulia cenderung sendirian sebagai atom bebas dan
setabil. Lewis dan Kossel mengamati bahwa konfigurasi elektron unsur gas mulia
terisi 8 elektron di kulit terluarnya (oktet), kecuali helium yang terisi 2 elektron.
Atom-atom unsur yang lain akan saling berikatan supaya setabil, yaitu agar kulit
terluarnya terisi 8 elektron seperti halnya gas mulia.
Ikatan kimia adalah gaya tarik-menarik antara atom-atom sehingga atom-
atom tersebut tetap berada bersama-sama dan terkombinasi dalam suatu
senyawaan. Ikatan antar atom dalam sebuah senyawa dapat terbentuk melalui serah
terima elektron kemudian terjadi gaya tarik elektrostatik antara ion positip dan ion
negatif yang terbentuk (terjadi ikatan ion), atau dengan cara tarik-menarik
pasangan elektron yang digunakan bersama (terjadi ikatan kovalen).
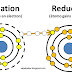
Ikatan Ion
Contoh: ikatan ion dalam NaCl terbentuk melalui gaya tarik elektrostatik antara ion
Na+ dan Cl-. Ion Na+ terbentuk dari atom Na yang melepaskan 1 elektron
terluarnya. Elektron yang dilepas tersebut diterima oleh atom Cl pada kulit
terluarnya, sehingga terbentu ion Cl-.
Na• Cl ——→ Na+ Cl–
Ikatan Kovalen
Contoh: ikatan kovalen dalam senyawa HCl terbentuk melalui penggunaan
bersama 1 elektron dari H dan 1 elektron terluar Cl.
H • • Cl atau dituliskan H―Cl
Ikatan kovalen dapat berupa ikatan kovalen tunggal, rangkap dua, atau rangkap
tiga.
Contoh ikatan kovalen tunggal : Cl―Cl
Contoh ikatan kovalen rangkap dua : O═O
Contoh ikatan kovalen rangkap tiga : N≡N
Pasangan elektron yang digunakan bersama bisa juga hanya berasal dari salah satu
atom yang berikatan. Ikatannya disebut kovalen koordinat, disimbulkan dengan
anak panah. Contoh dalam molekul NO2 dan NH4+.
H
│
O═N→O H─N→H+
│
H
Kepolaran Ikatan dan Keelektronegatifan
Jenis ikatan dapat ditentukan dari selisih keelektronegatifan atom-atom
yang berikatan. Jika selisihnya lebih dari 2, maka ikatannya bersifat ionik. Jika
selisihnya antara 0,5 dan 2, maka ikatannya bersifat kovalen polar. Jika selisihnya
kurang dari 0,5, maka ikatannya bersifat kovalen nonpolar. Sebetulnya tidak ada
ikatan yang murni ikatan ion. Umumnya ikatan ion juga memiliki sedikit sifat
ikatan kovalen. Begitupun sebaliknya.
Penyimpangan Aturan Oktet
Pada atom yang memiliki elektron terluarnya ganjil, dapat terjadi
penyimpangan dari aturan oktet, yaitu setelah berikatan jumlah elektron terluarnya
tidak 8 tetapi setabil. Jika jumlah elektron terluarnya masih kurang dari 8, maka
disebut oktet tak lengkap. Jika jumlah elektron terluarnya menjadi lebih dari 8,
maka disebut oktet berkembang.
Contoh oktet tak lengkap: