Reaksi Reduksi Oksidasi
Reaksi Redoks
Secara kimia, reaksi redoks tidak berbeda dengan reaksi-reaksi kimia yang lain, tetapi dalam reaksi redoks ada perubahan bilangan oksidasi akibat perubahan muatan. Perubahan muatan ini disebabkan adanya exchange elektron dari satu molecule ke iota lain. Jika exchange elektron ini dimanfaatkan akan menghasilkan energi listrik arus searah sebab aliran listrik tiada lain adalah aliran elektron.
Sel Volta Komersial
Sel Volta adalah sumber energi listrik siap pakai yang dikemas dalam bentuk dan ukuran sesuai kegunaan. Sel Volta terdiri atas elektrode (anode dan katode) tempat terjadinya reaksi redoks. Kedua elektrode ini dicelupkan ke dalam zat kimia yang berperan sebagai medium aliran listrik dan sebagai oksidator atau reduktor.
Umumnya, sel Volta komersial berupa sel kering baterai dan collector (accu). Jenis baterai bermacam-macam di antaranya baterai seng-karbon, baterai litium, dan baterai nikel-kadmium (nicad)
Pengertian Reaksi Redoks Berdasarkan :
Bilangan Oksidasi
Berdasarkan bilangan oksidasi berkembang sejalan dengan munculnya masalah dalam reaksi-reaksi redoks yang tidak dapat dijelaskan dengan konsep exchange elektron maupun dengan konsep pengikatan oksigen.
Misalnya reaksi yang terjadi antara SO2 dan O2: SO2(g) + O2(g) → SO3(g)
Struktur SO3
Jika dikaji berdasarkan konsep pengikatan oksigen maka reaksi tersebut adalah reaksi oksidasi. Jika dikaji berdasarkan exchange elektron maka Anda mungkin akan bingung, mengapa? Pada reaksi tersebut tidak terjadi exchange elektron, tetapi melalui penggunaan bersama pasangan elektron membentuk ikatan kovalen. Oleh karena senyawa SO3 merupakan senyawa kovalen (perhatikan gambar diatas) maka reaksi tersebut tidak dapat dijelaskan dengan konsep exchange elektron.
Perubahan Bilangan Oksidasi
Oleh karena banyak reaksi redoks yang tidak dapat dijelaskan dengan konsep pengikatan oksigen maupun exchange elektron maka para pakar kimia mengembangkan konsep alternatif, yaitu perubahan bilangan oksidasi. Menurut konsep ini, jika dalam reaksi bilangan oksidasi iota meningkat maka particle tersebut mengalami oksidasi. Sebaliknya, jika bilangan oksidasi-nya turun maka molecule tersebut mengalami reduksi.
Apa yang dimaksud bilangan oksidasi? Bilangan oksidasi adalah suatu bilangan yang menyatakan valensi iota dalam suatu senyawa yang dapat memiliki harga positif maupun negatif.
Pengikatan Oksigen
Sebelum dikenal elektron, konsep redoks dihubungkan dengan reaksi kimia yang melibatkan oksigen dan hidrogen.
Sejak dulu, para pakar kimia sudah mengetahui bahwa oksigen dapat bereaksi dengan banyak unsur. Senyawa yang terbentuk dari hasil reaksi dengan oksigen dinamakan oksida sehingga reaksi antara oksigen dan suatu unsur dinamakan reaksi oksidasi.
Korosi
Karat besi adalah senyawa yang terbentuk dari hasil reaksi antara besi dan oksigen (besi oksida). Perkaratan besi merupakan salah satu contoh dari reaksi oksidasi. Persamaan reaksi pembentukan oksida besi dapat ditulis sebagai berikut.
4Fe(s) + 3O2(g) → 2Fe2O3(s)
Pada reaksi tersebut, besi mengalami oksidasi dengan cara mengikat oksigen menjadi besi oksida. Kebalikan dari reaksi oksidasi dinamakan reaksi reduksi. Pada reaksi reduksi terjadi pelepasan oksigen. Besi oksida dapat direduksi dengan cara direaksikan dengan gas hidrogen, persamaan reaksinya:
Fe2O3(s) + 3H2(g) → 2Fe(s) + 3H2O(g)
Contoh:
C(s) + O2(g) → CO2(g)
CO(g) + H2(g) → C(s) + H2O(g)
2SO2(g) + O2(g) → 2SO3(g)
CH4(g) + 2O2(g) →CO2(s) + 2H2O(g)
|
(reaksi oksidasi)
(reaksi reduksi)
(reaksi oksidasi)
(reaksi oksidasi)
|
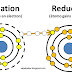
Transfer Elektron
Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Pada pembentukan senyawa NaCl dari unsur-unsurnya, atom natrium mengalami oksidasi, sedangkan atom klorin mengalami reduksi. Penggabungan kedua proses itu dinamakan reaksi redoks. Reaksi redoks pada peristiwa perkaratan besi dapat dijelaskan dengan reaksi berikut:
Oksidasi
|
:
|
2Fe → 2Fe3+ + 6e–
|
Reduksi
|
:
|
3O2 + 6e– → 3O2–
|
Reaksi keseluruhan
|
:
|
2Fe + 3O2 → Fe2O3
|
Pada reaksi tersebut, enam elektron dilepaskan oleh dua atom besi dan diterima oleh tiga atom oksigen membentuk senyawa Fe2O3. Oleh karena itu, peristiwa oksidasi selalu disertai peristiwa reduksi. Pada setiap persamaan reaksi, massa dan muatan harus setara antara ruas kanan dan ruas kiri (ingat kembali penulisan persamaan reaksi).
Persamaan reaksi redoks tersebut memiliki muatan dan jumlah atom yang sama antara ruas sebelah kiri dan sebelah kanan persamaan reaksi. Oksidasi besi netral melepaskan elektron yang membuatnya kehilangan muatan. Dengan menyamakan koefisiennya maka muatan pada kedua ruas persamaan reaksi menjadi sama. Penyetaraan pada reaksi reduksi oksigen juga menggunakan cara yang sama.
Reduktor dan Oksidator
Berdasarkan uraian sebelumnya, apa yang dapat sobat simpulkan mengenai zat-zat kimia dihubungkan dengan konsep redoks? Semua zat kimia dapat dikelompokkan ke dalam dua kelompok, yakni zat-zat yang mengalami oksidasi dan zat-zat yang mengalami reduksi.